Рассмотрим еще одну интересную статью от 2015 года (США):
«Распространенность и клинические корреляты короткого начала REM-периода (SOREMP) во время плановой полисомнографии» — «Prevalence and Clinical Correlates of a Short Onset REM Period (SOREMP) during Routine PSG»:
https://academic.oup.com/sleep/article/38/10/1575/2468599
Во первых, любопытно, что SOREMP здесь расшифровывается как Short Onset REM Period, а не Sleep-onset REM period. Что я больше почти нигде не нашел в научных статьях. Странно, что такая расшифровка аббревиатуры прошла рецензирование и с чем это связано, мне не известно. Может быть за этим стоит какая-то история. Интересно будет выяснить. Но не суть.
Что касается самой статьи, то в ней анализируется огромная выборка данных — 79651 пациент без Multiple Sleep Latency Test (MSLT) и 3059 с MSLT.
Результаты следующие (цитирую выводы):
SOREMPs редко встречаются в общей выборке по полисомнографическим наблюдениям (<1,0%), но являются высокоспецифичным¹ признаком для диагностики нарколепсии. Несмотря на общую редкость, распространенность этого явления намного выше предполагаемой распространенности нарколепсии и может предоставить практикующим врачам возможность идентифицировать нарколепсию у пациентов клиники сна. Эти данные также свидетельствуют о том, что при полисомнографических обследованиях на SOREMP для диагностики нарколепсии должно учитываться наличие сменной/ночной работы и/или других факторов, которые могут привести к нарушению фазы БДГ (включая апноэ и т. п. нарушения), что подтверждает существующие наблюдения о том, что нарушения сна и недостаточный и/или несвоевременный сон должны быть исключены и/или должным образом контролироваться перед проведением полисомнографического обследования.
¹ Напомню, что такое специфичность. Этот показатель определяет, в данном случае, насколько вероятно, что пациент без SOREMPs — НЕ нарколептик. То есть, если SOREMPs нет, то очень маловероятно, что у пациента нарколепсия. Или, другими словами — всегда, когда есть нарколепсия, то есть и SOREMPs. Но это не означает, что если есть SOREMPs, то у человека обязательно нарколепсия. Это другой статистический параметр — чувствительность. И про чувствительность в данном разделе ничего не говорится.
Далее я приведу фрагменты из автоперевода, но сначала вкратце о еще одной интересной диаграмме:
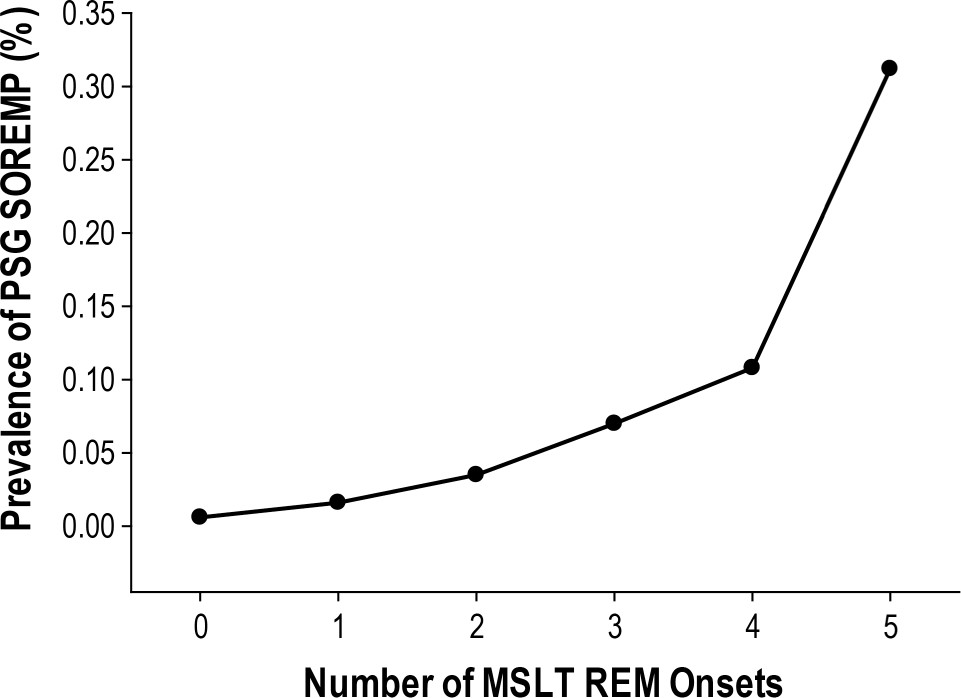
Здесь показана взаимосвязь количества SOREMPs во время MSLT (днем) и ночного SOREMP в первый цикл сна (при условии наступления фазы БДГ через 15 или менее минут после засыпания). И мы видим, что у тех пациентов, кто все 5 раз днем попадал на засыпании в фазу БДГ, в 33% случаев был SOREMPs и при засыпании вечером.
Подробности цитирую в формате автоперевода:
В целом, распространенность PSG-SOREMP среди тех, кто прошел MSLT на следующее утро, составила 1,8% (n = 54) и увеличивалась пропорционально количеству приступов БДГ при последовательной MSLT (от < 0,5% при отсутствии MSLT до > 33,0% для тех, у кого 5 MSLT REM; рисунок 1). Из 54 пациентов с ПСГ SOREMP окончательный диагноз был установлен только у 48 пациентов. Из этих 48 пациентов 37 (73%) поставили диагноз нарколепсия. Большинство диагнозов нарколепсии были без катаплексии (n = 33; 89%); только у 4 пациентов была диагностирована нарколепсия с катаплексией. В целом, наличие PSG-SOREMP было высокоспецифичным (99,5%; [95% ДИ: 99,1–99,7%]), но не чувствительным (6,7%; [95% ДИ: 4,7–9,2%]) в отношении нарколепсии. Положительные и отрицательные прогностические значения для PSG-SOREMP составили 77,9% (95% ДИ: 58,2–84,7%) и 83,7% (95% ДИ: 82,4–85,0%) соответственно. Восемь из 48 пациентов с ПСГ SOREMP получили диагноз гиперсомнии, 3 из которых имели только 1 SOREMP на MSLT (и, следовательно, потенциально могли квалифицироваться как нарколепсия в соответствии с ICSD-3).
Ну и еще одна интересная диаграмма. Это процент людей, у кого есть SOREMP при вечернем засыпании в целом, на выборке в 79651 пациент:
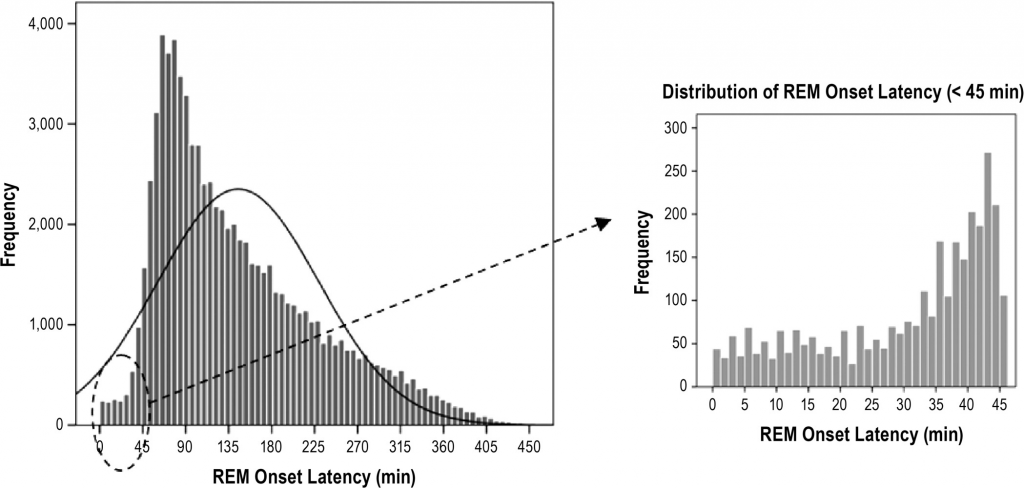
Мы видим, что у большинства людей фаза БДГ наступает через 45-90 минут после засыпания. Но у некоторых буквально в первые минуты. Вот эти первые 15 минут и считаются SOREMP, хотя на самом деле и 20, и даже 40 минут — это всё-таки довольно редко встречается.
Далее привожу просто выборочно автоперевод.
Введение
Нарколепсия представляет собой гетерогенное расстройство, характеризующееся нестабильной регуляцией сна/бодрствования, чрезмерной сонливостью, фрагментарным ночным сном и, в некоторых случаях, вторжением фазы быстрого сна в состояние бодрствования (катаплексия, гипногогические/гипнопомпические галлюцинации и сонный паралич 1 ). Ночные симптомы включают короткую задержку начала сна, снижение эффективности и качества сна, а также учащение переходов между состояниями. 2 При наличии катаплексии заболевание обычно вызывается разрушением нейропептидных гипокретиновых нейронов и тесно связано с положительным результатом на HLA DQB1*06:02. 3 , 4 Нарколепсия с катаплексией и без нее встречается редко (от 0,02% до 0,05% и примерно 0,2% соответственно 5 , 6 ).) и связано с повышенной заболеваемостью, снижением качества жизни и значительными медицинскими расходами. 7 , 8 Нарколепсия без катаплексии менее изучена, чем нарколепсия с катаплексией, и ее часто неправильно диагностируют как другие состояния сна/бодрствования. 9
До недавнего времени для диагностики нарколепсии в отсутствие катаплексии в соответствии с Международной классификацией расстройств сна, второе издание (ICSD-2) 9 требовался положительный результат (дневного) теста множественной латентности сна (MSLT) со средним значением латентность ≤ 8 минут и ≥ 2 периодов REM начала сна (SOREMP). Тем не менее, все больше данных связывают SOREMP при ночной полисомнографии (ПСГ) с нарколепсией. Это явление было впервые количественно определено Рехтшаффеном и его коллегами в 1963 году, когда они обнаружили, что примерно у 50% нарколептиков латентность БДГ ПСГ составляет ≤ 10 минут. 10 Совсем недавно Андлауэр и его коллеги 11обнаружили, что распространенность ПСГ SOREMP (определяемой как латентность REM ≤ 15 минут) у пациентов с подтвержденными случаями нарколепсии с катаплексией или дефицитом гипокретина колеблется от 35,7% до 57,4%. Эти статистические данные резко контрастируют с показателем менее 0,5% у пациентов без нарколепсии. 6 , 11 Более того, данные свидетельствуют о том, что ПСГ SOREMP является более специфичным (99,2% против 71,2%) и имеет более высокую положительную прогностическую ценность (92,1% против 75,0%) для подтвержденных случаев нарколепсии с дефицитом гипокретина, чем MSLT. 11
Эти данные вызвали изменение нозологии для диагностики нарколепсии, поскольку Международная классификация расстройств сна, третье издание (ICSD-3) 12 допускает, что SOREMP во время ПСГ засчитывается в один из ≥ 2 SOREMP, необходимых для последующего MSLT. Более того, DSM-5 предполагает, что SOREMP во время ПСГ достаточен для подтверждения диагноза нарколепсии без серии дневных снов MSLT. 13 Хотя данные показали, что ПСГ SOREMP является высокоспецифичным для подтвержденной нарколепсии с дефицитом гипокретина, информация о распространенности и клинических корреляциях в других популяциях, таких как клинические и общие популяции, ограничена из-за крайней редкости этого явления (4 в каждом случае). 1000 человек). 6 , 11Недавнее исследование, проведенное Голдбартом и его коллегами из Висконсинской когорты сна (n = 4866), показало, что распространенность SOREMP во время ПСГ лишь незначительно связана с продолжительностью сна предыдущей ночью, но предположило, что адекватная мощность не была достигнута из-за небольшого размера выборки. . 6
Это исследование преследовало две цели: (1) количественно оценить распространенность, чувствительность и специфичность ПСГ SOREMP (определяемую как латентность БДГ ≤ 15 мин) при нарколепсии у пациентов, которых оценивали на гиперсонливость с помощью последовательной MSLT, и (2) количественно оценить распространенность и предикторы SOREMP на исходной диагностической ПСГ в большой клинической выборке пациентов, тестируемых на различные нарушения сна.
Примеры различий и факторов, влияющих на PSG SOREMP
Как показано в Таблице 1 , пациенты в группе с подозрением на гиперсомнию (n = 3059) были моложе и стройнее (ИМТ) по сравнению с выборкой общей клиники сна. Выборка с подозрением на гиперсомнию также состояла в основном из женщин, где в общей клинической выборке распределение по полу было более равномерным. Также неудивительно, что пациенты в группе с подозрением на гиперсомнию с меньшей вероятностью имели признаки ОАС или ПЛМ. Эти различия выборок следует учитывать при интерпретации результатов, поскольку корректировка по возрасту, полу и ИМТ была невозможна из-за характера наборов данных.
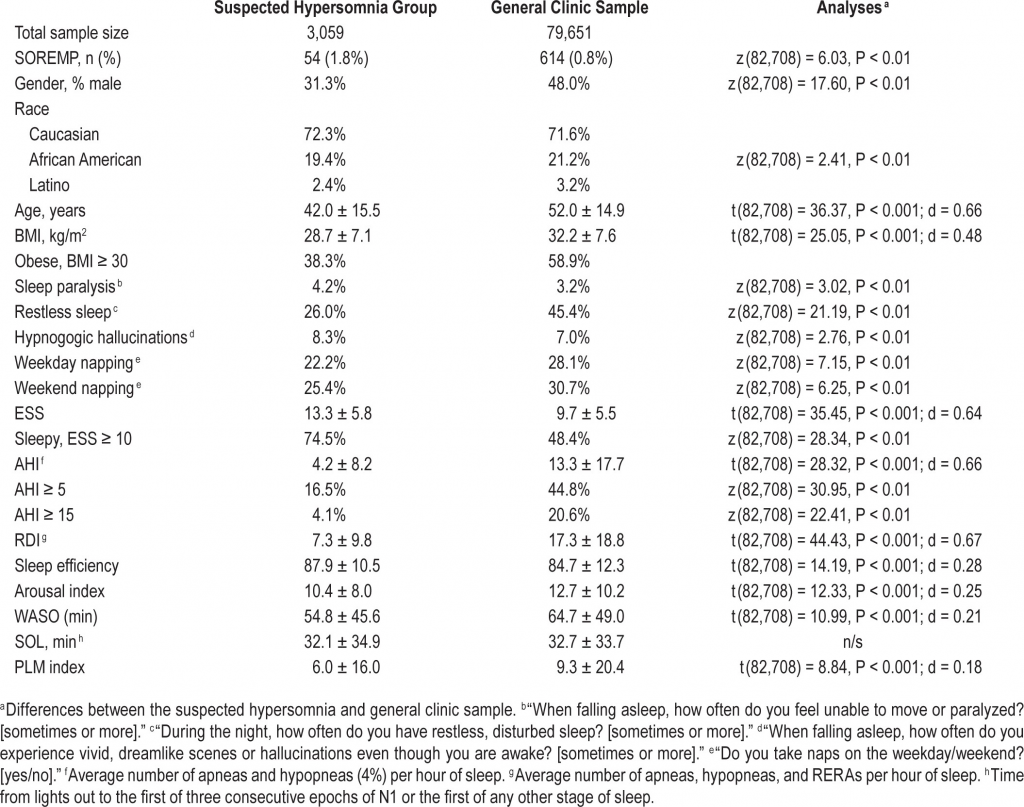
Распространенность ПСГ SOREMP была намного выше у тех, кто работал в ночное время и/или посменно, по сравнению с теми, кто работал днем. Этот вывод был последовательным как для выборки с подозрением на гиперсомнию (7,5% против 1,7%; ОШ: 4,4 [95% ДИ: 1,6–11,8]; χ 2 (8, 3,520) = 32,8, P <0,001), так и для выборки общей клинической картины . (2,1% против 0,9%; ОШ: 2,0 [95% ДИ: 1,6–2,7]; χ 2 (1, 156 654) = 28,5, P <0,001). Аналогичным образом, распространенность ПСГ SOREMP была выше у пациентов, перенесших титрование ПАП в общей клинической выборке (1,2% против 0,8%; ОШ: 1,3 [95% ДИ: 1,2–1,5]; χ 2 (8, 156 654) = 19,7, р<0,001). Основываясь на этих выводах, пациенты с любым из вышеперечисленных были исключены из окончательного анализа, чтобы уменьшить путаницу.
В целом, распространенность ПСГ SOREMP среди тех, кто прошел МСЛТ на следующее утро, составила 1,8% (n = 54) и увеличивалась пропорционально количеству приступов БДГ при последовательной МСЛТ (от < 0,5% при отсутствии МСЛТ до > 33,0% при те, у кого 5 MSLT REM, рисунок 1). Из 54 пациентов с ПСГ SOREMP окончательный диагноз был установлен только у 48 пациентов. Из этих 48 пациентов 37 (73%) поставили диагноз нарколепсия. Большинство диагнозов нарколепсии были без катаплексии (n = 33; 89%); только у 4 пациентов была диагностирована нарколепсия с катаплексией. В целом, наличие ПСГ SOREMP было высокоспецифичным (99,5%; [95% ДИ: 99,1–99,7%]), но не чувствительным (6,7%; [95% ДИ: 4,7–9,2%]) в отношении нарколепсии. Положительные и отрицательные прогностические значения для ПСГ SOREMP составили 77,9% (95% ДИ: 58,2–84,7%) и 83,7% (95% ДИ: 82,4–85,0%) соответственно. Восемь из 48 пациентов с ПСГ SOREMP получили диагноз гиперсомнии, 3 из которых имели только 1 начало REM на MSLT (и, следовательно, потенциально могли квалифицироваться как нарколепсия в соответствии с ICSD-3).
По сравнению с людьми с нормальной латентностью БДГ, пациенты с ПСГ SOREMP были старше, сонливее (по оценке ESS и латентности начала сна), имели больше признаков нарушения сна (субъективные и объективные) и с большей вероятностью имели умеренную или умеренную сонливость. тяжелый СОАС ( таблица 2 ). Любопытно, однако, что пациенты с ПСГ SOREMP не чаще сообщали о некоторых сопутствующих симптомах нарколепсии, включая гипногогические галлюцинации, сонный паралич и увеличение WASO. Самым надежным предиктором SOREMP PSG была афроамериканская раса. По сравнению с европеоидами у афроамериканцев вероятность наличия ПСГ SOREMP более чем в 4 раза выше, с учетом других значимых переменных в модели ( таблица 3 ).). В дополнение к расе, возраст и индекс возбуждения также объясняли уникальную дисперсию, но размеры эффекта, как правило, были небольшими. В сумме возраст, раса и индекс возбуждения объясняют 12,0% дисперсии в ПСГ SOREMP.
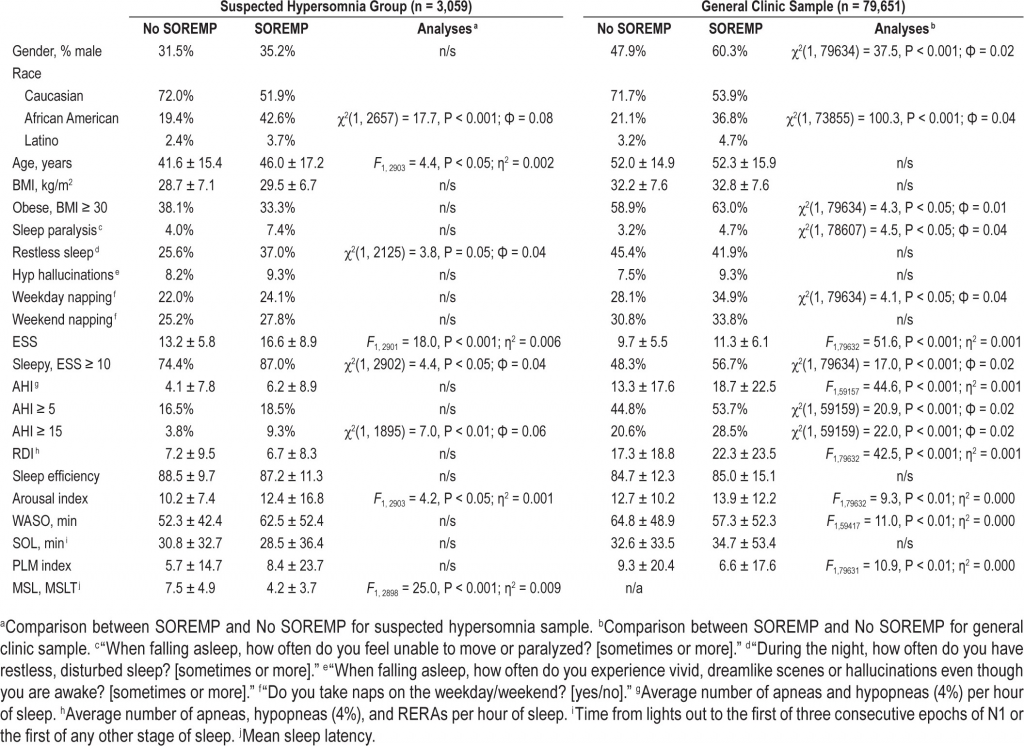

В среднем БДГ возникала через 145,1 ± 84,5 мин после начала сна, при этом у большинства пациентов БДГ длилась от 60 до 90 мин после начала сна ( рис. 2 ). Распространенность ПСГ SOREMP в этой выборке составила 0,8% ( таблица 1 ). Как и в случае с подозрением на гиперсомнию, пациенты с ПСГ SOREMP в общей клинической выборке были более сонливыми (согласно шкале сонливости Эпворта) и имели повышенный индекс возбуждения ( таблица 2 ).). Кроме того, в этой выборке пациенты с ПСГ SOREMP также чаще сообщали о регулярном дневном сне и сонном параличе по сравнению с пациентами с нормальной латентностью начала БДГ. Как и в группе с подозрением на гиперсомнию, наиболее надежным предиктором ПСГ SOREMP была афроамериканская раса. По сравнению с европеоидами афроамериканцы в 2,8 раза чаще имели ПСГ SOREMP с учетом других значимых переменных в модели ( таблица 3 ). Кроме того, в этой выборке мужской пол, дневной сон, WASO и OSA составляли уникальную дисперсию; однако общая объясненная дисперсия была небольшой и составляла 5%.
Обсуждение
Короткий латентный период БДГ-начала, определяемый как 15 минут или менее, редко встречается в клинических образцах сна в целом (< 1,0%), но является высокоспецифичным для нарколепсии, что подтверждает предыдущие данные Андлауэра и его коллег. 11 Несмотря на редкость, распространенность этого явления намного выше предполагаемой распространенности нарколепсии и может предоставить практикующим врачам важную возможность для выявления нарколепсии у пациентов клиники сна. Эти данные также свидетельствуют о том, что полезность ПСГ SOREMP для диагностики нарколепсии может зависеть от сменной/ночной работы в анамнезе и/или других факторов, которые могут привести к восстановлению фазы быстрого сна (например, прохождение титрования ПАП). Хорошо известно, что эти рабочие смены имеют повышенный уровень ложноположительных результатов на MSLT 6 , 19 .и интуитивно понятен, так как сменные/ночные работники, как правило, хронически ограничены во сне из-за смещения циркадных ритмов и нерегулярного режима работы по сравнению с нерабочим графиком сна. Это подтверждает опубликованные рекомендации о том, что другие нарушения сна и недостаточный и/или несвоевременный сон должны быть исключены или должным образом контролироваться до проведения исследования сна. 14
У пациентов с подозрением на гиперсомнию специфичность ПСГ SOREMP в отношении нарколепсии была очень высокой и составляла 99,5%. Эта статистика почти идентична той, что была обнаружена в выборке из 516 пациентов с подтвержденной нарколепсией (99,2%). 11 Эти результаты в сочетании с открытием того, что распространенность SOREMP полисомнографии увеличивалась пропорционально частоте начала REM при последовательных MSLT, и что скорректированные прогностические модели объясняли лишь небольшую дисперсию в SOREMP полисомнографии (т. е. что-то еще, по-видимому, было объясняя этот феномен), подтверждают значимость ПСГ SOREMP в выявлении нарколепсии. Кроме того, частота ложноположительных результатов была низкой и составляла 0,7%, что свидетельствует о том, что маловероятно, что пациент с ПСГ SOREMP непоставить диагноз нарколепсия. Однако чувствительность ПСГ SOREMP к нарколепсии очень низкая, что позволяет предположить, что пациенты с нарколепсией часто имеют нормальную латентность к БДГ; т.е. ≥ 93% случаев нарколепсии будут «пропущены», если в качестве диагностического индикатора использовать только ПСГ SOREMP. Однако важно отметить, что чувствительность ПСГ SOREMP в нашей выборке (6,7%) была намного ниже, чем у Andlauer et al. (50,6%) и может быть связано с различиями в методах подсчета баллов (автоматизированные/под наблюдением человека или вручную, как в Andlauer et al.) или, что более вероятно, в характеристиках выборки. В частности, наша клиническая выборка нарколепсии состояла из большинства случаев без катаплексии (например, только 8,3% выборки с подозрением на гиперсомнию с SOREMP ночью имели документированную катаплексию), в то время как выборка Andlauer et al.
Интересно, что у пациентов с ПСГ SOREMP присутствовали некоторые, но не все характеристики нарколепсии, в том числе некоторые признаки нарушения ночного сна (укороченное начало сна, увеличение WASO и снижение эффективности сна). Эти результаты любопытны, поскольку нарколепсия характеризуется неполным переключением сна и бодрствования, что приводит к быстрым переходам между состояниями и плохой непрерывности сна. 2Эти данные требуют дальнейшего изучения, но могут быть связаны с рядом причин, таких как метод подсчета, использованный для этих данных, неоднородность выборки, средство сравнения выборки и статистическая мощность. Вообще говоря, все сравнения были в «ожидаемом направлении», но не достигли статистической значимости. Это может быть связано с тем, что выборка PSG SOREMP состояла из гетерогенной смеси пациентов с нарколепсией с катаплексией и без нее, гиперсонливостью и другими состояниями сна/бодрствования и состояниями здоровья. Аналогичным образом были проведены статистические сравнения пациентов с различной степенью сна/бодрствования и заболеваниями, включая апноэ во сне и другие нарушения дыхания во сне, которые также могут прерывать непрерывность сна. Наконец, также возможно, что наш метод автоподсчета был недостаточно чувствителен, чтобы обнаруживать частые смены стадий. Другие клинические показатели, которые не дали последовательных прогностических результатов, включали симптомы гипногогических галлюцинаций и сонный паралич. Это может быть связано с рядом причин, в том числе упомянутых выше, а также с ограничениями, связанными с измерением, включая то, как вопросы оценивали такие симптомы и/или как вопрос был дихотомизирован («по крайней мере, иногда»). Также важно отметить, что, хотя гипногогические галлюцинации и сонный паралич являются сопутствующими признаками нарколепсии, они возникают не у всех пациентов с нарколепсией. На самом деле гипногогические галлюцинации возникают только у 28% пациентов с нарколепсией без катаплексии. включая упомянутые выше, а также ограничения, связанные с измерением, включая то, как вопросы оценивали такие симптомы и / или как вопрос был дихотомизирован («по крайней мере иногда»). Также важно отметить, что, хотя гипногогические галлюцинации и сонный паралич являются сопутствующими признаками нарколепсии, они возникают не у всех пациентов с нарколепсией. На самом деле гипногогические галлюцинации возникают только у 28% пациентов с нарколепсией без катаплексии. включая упомянутые выше, а также ограничения, связанные с измерением, включая то, как вопросы оценивали такие симптомы и / или как вопрос был дихотомизирован («по крайней мере иногда»). Также важно отметить, что, хотя гипногогические галлюцинации и сонный паралич являются сопутствующими признаками нарколепсии, они возникают не у всех пациентов с нарколепсией. На самом деле гипногогические галлюцинации возникают только у 28% пациентов с нарколепсией без катаплексии.20
Особое внимание следует уделить глубоким расовым различиям в распространенности ПСГ SOREMP. С учетом других факторов, которые, как было показано, влияют на SOREMP, афроамериканцы в обеих выборках примерно в 3–4 раза чаще имели ПСГ SOREMP, чем их европейские коллеги. В конечном счете, эти различия требуют дальнейшего изучения, поскольку нарколепсия может иметь расовые различия 21–23 .и может предоставить важную возможность для диагностики нарколепсии там, где в противном случае она могла бы остаться незамеченной. Например, данные свидетельствуют о том, что афроамериканцы, страдающие нарколепсией, как правило, менее склонны к катаплексии и могут быть более склонны к «атипичным» симптомам катаплексии (т. е. катаплексии в ответ на отрицательные, а не на положительные эмоции), несмотря на то, что они Риск гипокретина с низким уровнем спинномозговой жидкости в 20 раз выше, чем у представителей европеоидной расы. 24 , 25 Однако наши результаты могут быть также связаны с другими мешающими переменными, не оцениваемыми в этом исследовании, такими как различия во времени сна и / или обычной продолжительности сна. 6 , 24Например, большая национальная выборка из 29 818 взрослых показала, что у афроамериканцев на 35% повышен риск «экстремальной» продолжительности сна — как короткого (≤ 5 часов), так и длительного (≥ 9 часов). 24 Подобные расовые различия были обнаружены даже у маленьких детей. 26
Все выводы должны быть сделаны с учетом ограничений исследования. Основным ограничением было отсутствие доступа к информации о катаплексии (наилучший клинический показатель дефицита гипокретина), за исключением той, которая была доступна в окончательном диагнозе. Во-вторых, еще одним существенным ограничением было отсутствие данных о продолжительности обычного сна. Хорошо известно, что неадекватный и/или несвоевременный сон может увеличить вероятность преждевременного начала БДГ, как во время дневного сна 27 , так и ночью. 6 Например, согласно исследованию, проведенному Голбартом и его коллегами, каждый час уменьшения сна накануне вечером был связан с 34-процентным увеличением вероятности ночного SOREMP. 6Кроме того, важно отметить, что, поскольку скорректированный анализ учитывал очень небольшую дисперсию, можно предположить, что «что-то еще» управляло фенотипом. Конечно, это может быть истинная патология нарколепсии или другие переменные, такие как привычная продолжительность/время сна, лекарства и/или другие неизвестные факторы. Нарколепсия часто сочетается с несколькими заболеваниями и психическими расстройствами, 28 и лекарства для вышеупомянутых состояний часто имеют эффекты, подавляющие БДГ и/или другие эффекты, изменяющие архитектуру сна. 29 , 30Кроме того, возможно, что некоторые из этих пациентов использовали терапию или стимуляторы, стимулирующие бодрствование, которые могут изменить архитектуру сна. Наконец, были ограничения, связанные с нашей оценкой данных сна. Поскольку эти данные были обработаны с использованием метода автооценки, отредактированного человеком, не исключено, что период быстрого сна, особенно если он короткий и при отсутствии атонии (что нередко встречается у пациентов с нарколепсией 31 ), мог быть вообще пропустил. Эти данные подтверждают важность клинической корреляции и последующего наблюдения за пациентами с практикующим врачом, прошедшим обучение в области медицины сна, для пациентов, которые проходят обследование на предмет всех нарушений сна, особенно гиперсонливости и нарколепсии.